Электролиты — это… Что такое Электролиты?
жидкие или твёрдые вещества и системы, в которых присутствуют в сколько-нибудь заметной концентрации ионы, обусловливающие прохождение электрического тока. В узком смысле Э. называются вещества, растворы которых проводят электрический ток ионами, образующимися в результате электролитической диссоциации (См. Электролитическая диссоциация). Э. в растворах подразделяют на сильные и слабые. Сильные Э. практически полностью диссоциированы на ионы в разбавленных растворах. К ним относятся многие неорганические соли и некоторые неорганические кислоты и основания в водных растворах, а также в растворителях, обладающих высокой диссоциирующей способностью (спирты, амиды и др.). Молекулы слабых Э. в растворах лишь частично диссоциированы на ионы, которые находятся в динамическом равновесии с недиссоциированными молекулами. К слабым Э. относится большинство органических кислот и многие органические основания в водных и неводных растворах. Деление Э. на сильные и слабые в некоторой степени условно, т. к. оно отражает не свойства самих Э., а их состояние в растворе. Последнее зависит от концентрации, природы растворителя, температуры, давления и др.Свойства разбавленных растворов слабых Э. удовлетворительно описываются классической теорией электролитической диссоциации. Для не слишком разбавленных растворов слабых Э., а также для растворов сильных Э. эта теория неприменима, поскольку они являются сложными системами, состоящими из ионов, недиссоциированных молекул или ионных пар, а также более крупных агрегатов. Свойства таких растворов определяются характером взаимодействий ион-ион, ион-растворитель, а также изменением свойств и структуры растворителя под влиянием растворённых частиц. Современные статистические теории сильных Э. удовлетворительно описывают свойства лишь очень разбавленных (моль/л) растворов.
ЭЛЕКТРОЛИТЫ — это… Что такое ЭЛЕКТРОЛИТЫ?
в-ва, в к-рых в заметной концентрации присутствуют ионы, обусловливающие прохождение электрич. тока (ионную проводимость). Э. также наз. проводниками второго рода. В узком смысле слова Э.-в-ва, молекулы к-рых в р-ре вследствие электролитической диссоциации распадаются на ионы. Различают электролиты твердые, растворы электролитов
В соответствии с природой ионов, образующихся при электролитич. диссоциации водных р-ров, выделяют солевые Э. (в них отсутствуют ионы Н + и ОН —), к-ты (преобладают ионы Н +) и основания (преобладают ионы ОН —). Если при диссоциации молекул Э. число катионов совпадает с числом анионов, такие Э. наз. симметричными (1,1 -валентными, напр. КС1, 2,2-валентными, напр. CaSO4, и т. д.). В противном случае Э. наз. несимметричными (1,2-валентные Э., напр. H
По способности к электролитич. диссоциации Э. условно разделяют на сильные и слабые. Сильные Э. практически полностью диссоциированы на ионы в разбавленных р-рах. К ним относятся многие неорг. соли, нек-рые к-ты и основания в водных р-рах, а также в р-рителях, обладающих высокой диссоциирующей способностью (напр., в спиртах, амидах, кетонах). Молекулы слабых Э. лишь частично диссоциированы на ионы, к-рые находятся в динамич. равновесии с недиссоциир. молекулами. К слабым Э. относятся многие орг. к-ты и основания в водных и неводных р-рителях. Степень диссоциации зависит от природы р-рителя, концентрации р-ра, т-ры и др. факторов. Один и тот же Э. при одинаковой концентрации, но в разл. р-рителях образует р-ры с разл. степенью диссоциации.
Ионы в Э. являются отд. кинетич. единицами и участвуют в хим. р-циях и электрохим. процессах часто независимо от природы др. ионов, присутствующих в р-ре. При прохождении электрич. тока через Э. на погруженных в него электродах происходят окислит.-восстановит. р-ции, в результате чего в своб. виде выделяются в-ва, к-рые становятся компонентами Э. (см.
Э. по своей структуре представляют собой сложные системы, состоящие из ионов, окруженных молекулами р-рителя, недиссоциированных молекул растворенного в-ва, ионных пар и более крупных агрегатов. Св-ва Э. определяются характером ион-ионных и ион-молекулярных взаимод., а также изменением св-в и структуры р-рителя под влиянием растворенных частиц Э. В полярных р-рителях благодаря интенсивному взаимод. ионов с молекулами р-рителя образуются сольватные структуры (см.
В зависимости от концентрации Э. выделяют область разбавленных р-ров, к-рые по своей структуре близки к структуре чистого р-рителя, нарушаемой, однако, присутствием и влиянием ионов; переходную область и область концентрир. р-ров. Весьма разбавленные р-ры слабых Э. по своим св-вам близки к идеальным р-рам и достаточно хорошо описываются классич. теорией электролитич. диссоциации. Разбавленные р-ры сильных Э. заметно отклоняются от св-в идеальных р-ров, что обусловлено электростатич. межионным взаимод. Их описание проводится в рамках
В переходной концентрационной области под влиянием ионов происходит существенное изменение структуры р-рителя. При дальнейшем увеличении концентрации Э. почти все молекулы р-рителя связаны с ионами в сольватационные структуры и обнаруживается дефицит р-рителя, а в области концентрированных р-ров структура р-ра все более приближается к структуре соответствующих ионных расплавов или кристаллосольватов. Данные компьютерного моделирования и спектроскопич. исследований, в частности методом рассеяния нейтронов с изотопным замещением, свидетельствуют о значит. степени упорядоченности в концентрированных р-рах Э. и об образовании специфич. для каждой конкретной системы ионных структур. Напр., для водного р-ра NiCl
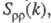
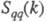 и
и 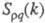 , описывающими флуктуации ионной плотности
, описывающими флуктуации ионной плотности 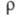 и заряда qкак ф-ции волнового числа k, к-рое с точностью до постоянной Планка hсовпадает с величиной импульса, передоваемого расплаву рассеивающей частицей, напр. нейтроном. Для бинарного электролита
и заряда qкак ф-ции волнового числа k, к-рое с точностью до постоянной Планка hсовпадает с величиной импульса, передоваемого расплаву рассеивающей частицей, напр. нейтроном. Для бинарного электролита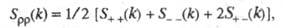
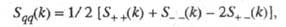
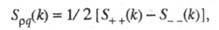
где 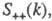
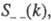
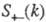 — парциальные структурные факторы, относящиеся к взаимод. катионов и анионов между собой и друг с другом. Для расплавов типа NaCl ф-ция
— парциальные структурные факторы, относящиеся к взаимод. катионов и анионов между собой и друг с другом. Для расплавов типа NaCl ф-ция 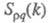
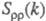 , а вторая -«зарядовым» упорядочением через ф-цию
, а вторая -«зарядовым» упорядочением через ф-цию 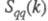 . Ф-ция
. Ф-ция 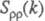 имеет типичное поведение для систем с «плотностным» упорядочением, отражая значит. степень беспорядка в расположении частиц. В отличие от этого
имеет типичное поведение для систем с «плотностным» упорядочением, отражая значит. степень беспорядка в расположении частиц. В отличие от этого 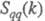 имеет резкий пик, отражающий сильное упорядочение в распределении заряда, определяемое экранированием и требованиями локальной электронейтральности. Такое упорядочение ионов приводит к возможности существования в Э. коллективных возбуждений, к-рые могут проявляться в виде пиков динамич. структурного фактора
имеет резкий пик, отражающий сильное упорядочение в распределении заряда, определяемое экранированием и требованиями локальной электронейтральности. Такое упорядочение ионов приводит к возможности существования в Э. коллективных возбуждений, к-рые могут проявляться в виде пиков динамич. структурного фактора 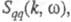 описывающего динамику флуктуации плотности заряда расплава (
описывающего динамику флуктуации плотности заряда расплава (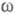 — частота, связанная с энергией, передаваемой расплаву рассеивающей частицей). Для ионных расплавов Э., катионы к-рых склонны к образованию ковалентных связей с анионами (напр., для расплава CuCl), наблюдается сильная корреляция взаимод. между анионами и довольно слабая — между катионами.
— частота, связанная с энергией, передаваемой расплаву рассеивающей частицей). Для ионных расплавов Э., катионы к-рых склонны к образованию ковалентных связей с анионами (напр., для расплава CuCl), наблюдается сильная корреляция взаимод. между анионами и довольно слабая — между катионами. Переход от одной концентрационной области Э. в другую происходит плавно, вследствие чего рассмотренное выше деление является условным. Тем не менее в промежут. области нек-рые термодинамич. св-ва Э., напр. коэф. р-римости, претерпевают заметные изменения. Описание промежут. и концентрационной областей требует явного рассмотрения как ионов, так и молекул р-рителя и учета разл. видов взаимод. между всеми частицами в р-ре.
В зависимости от т-ры и давления выделяют низкотемепературную и высокотемпературную области св-в Э., а также области нормальных и высоких давлений. Повышение т-ры или давления в целом снижают мол. упорядоченность р-рителя и ослабляет влияние ассоциативных и сольватационных эффектов на св-ва р-ра Э. При понижении т-ры иже т-ры плавления нек-рые концентрир. Э. могут находиться стеклообразном состоянии, напр. водные р-ры LiCl.
Наряду с Э. как проводниками второго рода существуют в-ва, обладающие одновременно электронной и ионной проводимостью. К ним относятся р-ры щелочных и щел.-зем. металлов в полярных р-рителях (аммиак, амины, эфиры), а также в расплавах солей. В этих системах при изменении концентрации металла происходит фазовый переход в металлич. состояние с существенным (на неск. порядков) изменением электропроводности. При этом в электролитич. области образуется самый легкий анион -сольватированный электрон, придающий р-ру характерный синий цвет.
Э. играют важную роль в науке и технике. Они участвуют в электрохим. и многих биол. процессах, являются средой для орг. и неорг. синтеза и электрохим. произ-в. Изучение св-в Э. важно для выяснения механизмов электролиза, электрокатализа, электрокристаллизации, коррозии металлов и др., для совершенствования механизмов разделения в-в — экстракции и ионного обмена. Исследование св-в Э. стимулируется энергетич. проблемами (создание новых топливных элементов, солнечных батарей, электрохимических преобразователей информации), а также проблемами защиты окружающей среды.
Лит.: Харнед Г., Оуэн Б., Физическая химия растворов электролитов, пер. с англ., М., 1952; Термодинамика и строение растворов. Материалы симпозиума «Химия водных систем при высоких температурах и давлениях», Иваново, 1986; March N.H., Тоsi M. P., Coulomb liquids, L.-[a.o.], 1984; см. также лит. к ст. Растворы электролитов, Электропроводность электролитов, Электролиты неводные, Электролиты твердые.
М. Ф. Головко.
Химическая энциклопедия. — М.: Советская энциклопедия. Под ред. И. Л. Кнунянца. 1988.
электролит — это… Что такое электролит?
электролит — электролит … Орфографический словарь-справочник
ЭЛЕКТРОЛИТ — (греч.). Жидкое тело, разлагаемое при помощи электрического (гальванического) тока. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. ЭЛЕКТРОЛИТ Жидкость, подверженная разложению посредством гальванического тока.… … Словарь иностранных слов русского языка
электролит — а, м. électrolyte m. < électro + гр. lytos разлагаемый. спец. Химическое вещество (в расплаве или растворе), способное разлагаться на составные части при прохождении через него электрического тока. Электролит аккумулятора. БАС 1. Швыряло… … Исторический словарь галлицизмов русского языка
электролит — Раствор, в котором при прохождении через него электрического тока происходит разложение вещества, которое приводит к появлению электрического тока. Электролит является основой аккумуляторов и батарей. [Гипертекстовый энциклопедический словарь по… … Справочник технического переводчика
ЭЛЕКТРОЛИТ — ЭЛЕКТРОЛИТ, раствор или расплав солей, способный проводить электрический ток и используемый для ЭЛЕКТРОЛИЗА (в ходе которого он разлагается). Ток в электролитах проводится заряженными частицами ИОНАМИ, а не электронами. Например, в свинцово… … Научно-технический энциклопедический словарь
ЭЛЕКТРОЛИТ — ЭЛЕКТРОЛИТ, электролита, муж. (от слова электрический и греч. lytos растворенный) (физ.). Раствор какого нибудь вещества, способного разлагаться на составные части при электролизе. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
электролит — сущ., кол во синонимов: 1 • католит (1) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
Электролит — Электролитами называют вещества, растворы и сплавыкоторых с другими веществами электролитически проводят гальваническийток. Признаком электролитической проводимости в отличие от металлическойдолжно считать возможность наблюдать химическое… … Энциклопедия Брокгауза и Ефрона
электролит — – вещество, водный раствор или расплав которого проводит электрический ток. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
ЭЛЕКТРОЛИТ — вещество, водный раствор или расплав которого проводит электрический ток (см.), образующимися в результате электролитической (см.). Этим Э., называемые также (см.) второго рода, отличаются от металлов (проводников первого рода), в которых перенос … Большая политехническая энциклопедия
Электролит — Электролит вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы, однако само вещество электрический ток не проводит. Примерами электролитов могут служить растворы кислот, солей и оснований.… … Википедия
ЭЛЕКТРОЛИТ — это… Что такое ЭЛЕКТРОЛИТ?
электролит — электролит … Орфографический словарь-справочник
ЭЛЕКТРОЛИТ — (греч.). Жидкое тело, разлагаемое при помощи электрического (гальванического) тока. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. ЭЛЕКТРОЛИТ Жидкость, подверженная разложению посредством гальванического тока.… … Словарь иностранных слов русского языка
электролит — а, м. électrolyte m. < électro + гр. lytos разлагаемый. спец. Химическое вещество (в расплаве или растворе), способное разлагаться на составные части при прохождении через него электрического тока. Электролит аккумулятора. БАС 1. Швыряло… … Исторический словарь галлицизмов русского языка
электролит — Раствор, в котором при прохождении через него электрического тока происходит разложение вещества, которое приводит к появлению электрического тока. Электролит является основой аккумуляторов и батарей. [Гипертекстовый энциклопедический словарь по… … Справочник технического переводчика
ЭЛЕКТРОЛИТ — ЭЛЕКТРОЛИТ, раствор или расплав солей, способный проводить электрический ток и используемый для ЭЛЕКТРОЛИЗА (в ходе которого он разлагается). Ток в электролитах проводится заряженными частицами ИОНАМИ, а не электронами. Например, в свинцово… … Научно-технический энциклопедический словарь
электролит — сущ., кол во синонимов: 1 • католит (1) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
Электролит — Электролитами называют вещества, растворы и сплавыкоторых с другими веществами электролитически проводят гальваническийток. Признаком электролитической проводимости в отличие от металлическойдолжно считать возможность наблюдать химическое… … Энциклопедия Брокгауза и Ефрона
электролит — – вещество, водный раствор или расплав которого проводит электрический ток. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
ЭЛЕКТРОЛИТ — вещество, водный раствор или расплав которого проводит электрический ток (см.), образующимися в результате электролитической (см.). Этим Э., называемые также (см.) второго рода, отличаются от металлов (проводников первого рода), в которых перенос … Большая политехническая энциклопедия
Электролит — Электролит вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы, однако само вещество электрический ток не проводит. Примерами электролитов могут служить растворы кислот, солей и оснований.… … Википедия
ЭЛЕКТРОЛИТ — это… Что такое ЭЛЕКТРОЛИТ?
электролит — электролит … Орфографический словарь-справочник
ЭЛЕКТРОЛИТ — (греч.). Жидкое тело, разлагаемое при помощи электрического (гальванического) тока. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. ЭЛЕКТРОЛИТ Жидкость, подверженная разложению посредством гальванического тока.… … Словарь иностранных слов русского языка
электролит — а, м. électrolyte m. < électro + гр. lytos разлагаемый. спец. Химическое вещество (в расплаве или растворе), способное разлагаться на составные части при прохождении через него электрического тока. Электролит аккумулятора. БАС 1. Швыряло… … Исторический словарь галлицизмов русского языка
электролит — Раствор, в котором при прохождении через него электрического тока происходит разложение вещества, которое приводит к появлению электрического тока. Электролит является основой аккумуляторов и батарей. [Гипертекстовый энциклопедический словарь по… … Справочник технического переводчика
ЭЛЕКТРОЛИТ — ЭЛЕКТРОЛИТ, раствор или расплав солей, способный проводить электрический ток и используемый для ЭЛЕКТРОЛИЗА (в ходе которого он разлагается). Ток в электролитах проводится заряженными частицами ИОНАМИ, а не электронами. Например, в свинцово… … Научно-технический энциклопедический словарь
ЭЛЕКТРОЛИТ — ЭЛЕКТРОЛИТ, электролита, муж. (от слова электрический и греч. lytos растворенный) (физ.). Раствор какого нибудь вещества, способного разлагаться на составные части при электролизе. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
электролит — сущ., кол во синонимов: 1 • католит (1) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
Электролит — Электролитами называют вещества, растворы и сплавыкоторых с другими веществами электролитически проводят гальваническийток. Признаком электролитической проводимости в отличие от металлическойдолжно считать возможность наблюдать химическое… … Энциклопедия Брокгауза и Ефрона
электролит — – вещество, водный раствор или расплав которого проводит электрический ток. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
Электролит — Электролит вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы, однако само вещество электрический ток не проводит. Примерами электролитов могут служить растворы кислот, солей и оснований.… … Википедия
Твёрдые электролиты — это… Что такое Твёрдые электролиты?
Твёрдые электроли́ты (суперионные проводники) — кристаллические вещества с ионной природой химической связи, имеющие высокую электрическую проводимость, обусловленную движением ионов одного типа.
У суперионных проводников электропроводность при комнатной температуре составляет величину порядка 10-1 Ом-1·см-1, сравнимую с электропроводностью расплавов и концентрированных растворов жидких электролитов. Но, в отличие от металлов, проводимость которых осуществляется за счёт свободных электронов, и жидких электролитов, проводимость которых определяют как анионы, так и катионы, в твёрдых электролитах проводимость обусловлена перемещением ионов одного типа. Твёрдые электролиты сочетают свойства жидкостей (проводимость, характерную для жидкого расплава или раствора, ионную термоэдс) и твёрдых тел (механическую жесткость кристаллов).
Возможность суперионной проводимости во многом зависит от структурных особенностей материала. Большинство твёрдых электролитов — твёрдые растворы на основе ионных кристаллов. В узлах кристаллической решётки ионных кристаллов находятся заряженные ионы, образующие две подрешётки — катионную и анионную, атомы в которых, совершая колебательные движения, перемещаться по кристаллу не могут. Кристаллы со статистическим (неупорядоченным) расположением ионов по узлам решётки обладают особенно высокой ионной проводимостью. Когда количество ионов оказывается меньше количества узлов, то есть имеются вакансии, многие узлы оказываются свободными, что облегчает вероятность перескока иона из одного узла в другой. К кристаллам такого типа относятся AgI, Ag4RbI5, Ag2S, LiI и т. д. Например, в элементарной ячейке AgI на 42 позиции приходятся 2 иона Ag+, причем 12 тетраэдрических позиций являются предпочтительными. Таким образом подрешётка ионов проводимости разупорядочена, в то время как остальные ионы образуют жёсткий каркас, и их перенос возможен по обычным механизмам образования точечных дефектов (вакансий и междоузельных ионов). Ионная составляющая общей проводимости ТВЁРДЫХ ЭЛЕКТРОЛИТОВ, как правило, на 5-6 порядков больше электронной, то есть числа переноса (см. Электропроводность электролитов) ионов проводимости практически равны 1. Коэффиценты диффузии D этих ионов сравнимы с таковыми для концентрированных водных растворов и соответствуют величинам порядка 10-5 — 10-6 см2/с.
ЭЛЕКТРОЛИТЫ ТВЁРДЫЕ относят к супер-ионным проводникам и часто называют супериониками. Однако супер-ионик более общее понятие, относящееся к высокопроводящим соединениям как с ионной проводимостью, так и со смешанной ионно-электронной проводимостью. В электрохимический системах в отличие от ТВЁРДЫХ ЭЛЕКТРОЛИТОВ т.н суперионики со смешанной проводимостью выполняют роль электродов.
Если же в твёрдом электролите искусственно создать разупорядочение кристаллической решётки по одному из типов, например, в основное вещество ввести соединение, в котором анионов меньше, а катионов — столько же, в анионной подрешётке появляются вакансии, которые в отрицательно заряженной решётке можно рассматривать как положительные заряды.
Под действием внешнего напряжения в них начнут переходить анионы с достаточно большой энергией, а вакансии будут перемещаться в противоположном направлении. Возникнет электрический ток, обусловленный движением ионов только одного сорта. Но чтобы ионы могли перемещаться, энергетически близких кристаллографических позиций для размещения потенциально подвижных ионов в элементарной ячейке должно быть больше, чем самих ионов. Ионная проводимость зависит от концентрации вакансий. Но одновременно с ростом концентрации вакансий уменьшается подвижность ионов. В твёрдых растворах оксидов металлов разной валентности ток создается отрицательными ионами (анионами) кислорода. Твёрдые электролиты на основе оксидных металлов относятся к высокотемпературным электролитам. При комнатной температуре твёрдые электролиты на основе оксидных металлов проявляют свойства обычного изолятора. При нагреве подвижность анионов увеличивается очень быстро. Основная рабочая температура твёрдых электролитов на основе оксидных металлов находится в пределах между 700 и 1000°С.
Кроме твёрдых электролитов на основе ионных соединений существуют твёрдые полимерные электролиты — полимеры, в состав молекул которых входят функциональные группы, способные к диссоциации с образованием катионов или анионов, направленное движение которых внутри структуры полимера обусловливает его ионную проводимость.
ЭЛЕКТРОЛИТЫ ТВЁРДЫЕ подразделяются на электролиты с собственным структурным разупорядочением в одной из подрешёток и с примесным. К первым относятся вещества, структура которых либо уже имеет пути проводимости для ионов определённого типа, как, например, Na- -глинозем (полиалюминат натрия Na1+xAl11O17), либо приобретает их вследствие фазового перехода, как, например, AgI (β-α-переход при 420 К). Пути проводимости могут иметь вид каналов [например, в (C5H5NH)Ag5I6], щелей (например, в Na-β-глиноземе) или трехмерных сеток (например, в α-Agl).
К ТВЁРДЫМ ЭЛЕКТРОЛИТАМ с примесным разупорядочением относятся твёрдые растворы замещения, образующиеся в ионных кристаллах при легировании их ионами с валентностью, отличной от валентности основного иона. Возникающий при этом дефицит (или избыток) заряда компенсируется образованием дефектов противоположного знака. Так, в оксидах Zr, Hf, Се и Th, легированных оксидами двух- и трехвалентных металлов (Са, Y, Sc и др.), компенсация заряда примеси осуществляется кислородными вакансиями. Фторид кальция CaF2 и изоморфный ему SrF2 образуют с фторидами трехвалентных РЗЭ твёрдые растворы замещения, обладающие высокой подвижностью ионов F—. Последние легко обмениваются на ионы О2-.
Характерное свойство ТВЁРДЫХ ЭЛЕКТРОЛИТОВ — способность к замещению одних ионов проводимости на другие. Например, при выдерживании Na-β-глинозема в расплаве AgNO3 ионы Na+ может быть полностью замещены ионами Ag+. Если же Ag-β-глинозем поместить в раствор кислоты, то можно получить глинозем с высокой проводимостью по протонам — ионам Н+.
http://www.xumuk.ru/encyklopedia/2/5308.html
электролит — это… Что такое электролит?
электролит — электролит … Орфографический словарь-справочник
ЭЛЕКТРОЛИТ — (греч.). Жидкое тело, разлагаемое при помощи электрического (гальванического) тока. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. ЭЛЕКТРОЛИТ Жидкость, подверженная разложению посредством гальванического тока.… … Словарь иностранных слов русского языка
электролит — а, м. électrolyte m. < électro + гр. lytos разлагаемый. спец. Химическое вещество (в расплаве или растворе), способное разлагаться на составные части при прохождении через него электрического тока. Электролит аккумулятора. БАС 1. Швыряло… … Исторический словарь галлицизмов русского языка
электролит — Раствор, в котором при прохождении через него электрического тока происходит разложение вещества, которое приводит к появлению электрического тока. Электролит является основой аккумуляторов и батарей. [Гипертекстовый энциклопедический словарь по… … Справочник технического переводчика
ЭЛЕКТРОЛИТ — ЭЛЕКТРОЛИТ, раствор или расплав солей, способный проводить электрический ток и используемый для ЭЛЕКТРОЛИЗА (в ходе которого он разлагается). Ток в электролитах проводится заряженными частицами ИОНАМИ, а не электронами. Например, в свинцово… … Научно-технический энциклопедический словарь
ЭЛЕКТРОЛИТ — ЭЛЕКТРОЛИТ, электролита, муж. (от слова электрический и греч. lytos растворенный) (физ.). Раствор какого нибудь вещества, способного разлагаться на составные части при электролизе. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
электролит — сущ., кол во синонимов: 1 • католит (1) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
Электролит — Электролитами называют вещества, растворы и сплавыкоторых с другими веществами электролитически проводят гальваническийток. Признаком электролитической проводимости в отличие от металлическойдолжно считать возможность наблюдать химическое… … Энциклопедия Брокгауза и Ефрона
электролит — – вещество, водный раствор или расплав которого проводит электрический ток. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
ЭЛЕКТРОЛИТ — вещество, водный раствор или расплав которого проводит электрический ток (см.), образующимися в результате электролитической (см.). Этим Э., называемые также (см.) второго рода, отличаются от металлов (проводников первого рода), в которых перенос … Большая политехническая энциклопедия
Электролит — Электролит вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы, однако само вещество электрический ток не проводит. Примерами электролитов могут служить растворы кислот, солей и оснований.… … Википедия
