Электролит — это… Что такое Электролит?
Электроли́т — вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы, однако само вещество электрический ток не проводит. Примерами электролитов могут служить растворы кислот, солей и оснований. Электролиты — проводники второго рода, вещества, которые в растворе (или расплаве) состоят полностью или частично из ионов и обладающие вследствие этого ионной проводимостью.
Степень диссоциации
В растворах некоторых электролитов диссоциирует лишь часть молекул. Для количественной характеристики электролитической диссоциации было введено понятие степени диссоциации[1].
Классификация
Исходя из степени диссоциации все электролиты делятся на две группы
- Сильные электролиты — электролиты, степень диссоциации которых в растворах равна единице (то есть диссоциируют полностью) и не зависит от концентрации раствора. Сюда относятся подавляющее большинство солей, щелочей, а также некоторые кислоты (сильные кислоты, такие как: HCl, HBr, HI, HNO
- Слабые электролиты — степень диссоциации меньше единицы (то есть диссоциируют не полностью) и уменьшается с ростом концентрации. К ним относят воду, ряд кислот (слабые кислоты), основания p-, d-, и f- элементов.
Между этими двумя группами четкой границы нет, одно и то же вещество может в одном растворителе проявлять свойства сильного электролита, а в другом — слабого.
Использование термина
В естественных науках
Термин электролит широко используется в биологии и медицине. Чаще всего подразумевают водный раствор, содержащий те или иные ионы (напр., «всасывание электролитов» в кишечнике).
В технике
Слово электролит широко используется в науке и технике, в разных отраслях оно может иметь различающийся смысл.
В электрохимии
Многокомпонентный раствор для электроосаждения металлов, а также травления и др. (технический термин, например, электролит золочения).
В источниках тока
Электролиты являются важной частью химических источников тока: гальванических элементов и аккумуляторов.[2] Электролит участвует в химических реакциях окисления и восстановления с электродами, благодаря чему возникает ЭДС. В источниках тока электролит может находиться в жидком состоянии (обычно это — водный раствор), или загущённым до состояния геля.
Электролитический конденсатор
В электролитических конденсаторах в качестве одной из обкладок используется электролит. В качестве второй обкладки — металлическая фольга (алюминий), или пористый, спечённый из металлических порошков блок (тантал, ниобий). Диэлектриком в таких кондесаторах служит слой оксида самого металла, формируемый химическими методами на поверхности металлической обкладки.
Конденсаторы данного типа, в отличие от других типов, обладают несколькими отличительными особенностями:
- Высокая объемная и весовая удельная ёмкость.
- Требование к полярности подключения в цепях постоянного напряжения. Несоблюдение полярности вызывает бурное вскипание электролита, приводящее к механическому разрушению корпуса конденсатора (взрыву).
- Значительные утечки и зависимость электрической ёмкости от температуры.
- Ограниченный сверху диапазон рабочих частот (типовые значения сотни кГц … десятки МГц в зависимости от номинальной ёмкости и технологии).
Примечания
- ↑ Степень диссоциации (α) — отношение числа молекул, диссоциировавших на ионы к общему числу молекул растворенного электролита.
- ↑ ГОСТ 15596-82 Источники тока химические. Термины и определения
| B05A |
| ||
|---|---|---|---|
| B05B |
| ||
| B05C |
| ||
| B05D |
| ||
| B05X |
| ||
| B05Z |
Что такое электролит для аккумуляторов и как его приготовить?

Электролит – одна из основных составляющих аккумуляторных батарей, которые дают возможность запуска автомобиля. Он бывает нескольких видов, различающихся по своему составу. Своевременный контроль за количеством и качеством электролита в аккумуляторе позволит избежать преждевременный выход аккумулятора из строя и сэкономить на покупке нового устройства.
Содержание статьи
Виды, состав и особенности
На данный момент различают три вида электролитов для аккумуляторов, для щелочных аккумуляторов — щелочной, а для кислотных — кислотный, но так же выделяют и корректирующий электролит, необходимый при обслуживании батарей.
Как определить кислотный аккумулятор или щелочной? Проще всего это сделать по маркировке корпуса и по материалу, из которого он сделан. Корпус кислотных АКБ всегда изготавливается из специального пластика, тогда как щелочные батареи могут быть сделаны из металла. Так же можно определить протестировав каплю электролита из аккумулятора: кислотный электролит вступит в реакцию с содой или мелом.
Кислотный
Представляет собой смесь серной кислоты, составляющей тридцать пять процентов всего состава, и дистиллированной воды, которая занимает оставшиеся шестьдесят пять.  Данный состав в аккумуляторе находится в емкости со свинцовыми пластинами, при контакте этих элементов и происходит выработка тока.
Данный состав в аккумуляторе находится в емкости со свинцовыми пластинами, при контакте этих элементов и происходит выработка тока.
Преимущества кислотного электролита:
- Высокий уровень КПД
- Слабая потеря заряда при бездействии
- Выдача высокого стартового тока
- Невысокая стоимость
Недостатки:
- Чувствительность к перепадам температур
- Неэкологичность
- Необходимость регулярного контроля плотности состава
Следует отметить, что кислотный электролит используется в большинстве моделей аккумуляторных батарей для автомобилей, так как только он способен давать достаточное количество тока для запуска двигателя. При этом аккумуляторы, изготовленные с использованием данного раствора, делятся на две группы:
- Обслуживаемые
- Необслуживаемые
Первый вид обеспечивает легкий доступ к содержимому банок. В них можно замерять плотность электролита, при необходимости заливать дистиллированную воду и электролит, просто открутив крышки с банок.
В случае с необслуживаемыми моделями провести подобные действия также возможно, однако для этого нужно самостоятельно вскрыть устройство, провести нужные действия, а затем герметично их закрыть. В подобных случаях могут быть использованы дрель и сварочный аппарат.
Проводить замену электролита в необслуживаемых моделях стоит только в тех случаях, когда их гарантийный срок истек. Часто это производится исключительно для получения опыта проведения подобных операций.
Щелочной
Щелочной электролит состоит из гидроокиси калия, натрия, лития или всех этих составляющих в комплексе, разведенных в воде.
К достоинствам данного вида относятся:
- Длительный период службы
- Способность сохранять свойства при значительных перепадах температуры
- Гораздо меньшее выделение вредных газов в атмосферу
- Способность выдерживать встряски
- Неприхотливость в обслуживании

Недостатки:
- Меньшая величина электродвижущей силы по сравнению с кислотными
- Отсутствие способности подачи стартового тока для запуска двигателя
- Более высокая стоимость
Несмотря на долгий срок службы, неприхотливость и другие преимущества применение данного вида электролита в автомобильной промышленности ограничено. Виной тому неспособность выработки достаточного уровня стартового тока, необходимого для запуска двигателя. К минусам также относятся их внушительные габариты.
Однако устройства на щелочном электролите успешно применяются в обеспечении током тяговых и локомотивных составов.
Важно! Перед осуществлением замены следует убедиться, что аккумулятор именно щелочной. В противном случае АКБ можно полностью вывести из строя.
Корректирующий
Данный электролит является специальным составом с высоким содержанием активных веществ, используемый для повышения плотности электролита аккумулятора. Он предназначен для повышения концентрации активных веществ в батарее. 
В продаже можно встретить следующие виды корректирующего электролита:
- Твердый калиево-литиевый
- Жидкий калиево-литиевый с различной плотностью
- Жидкий кислотный
Корректирующий электролит можно изготовить самостоятельно
Как пользоваться корректирующим электролитом:
- Удалить из банок немного электролита
- Долить в них такое же количество корректирующей жидкости
- Установить АКБ на заряд номинальным током для запуска процесса смешивания полученного состава на полчаса
- Оставить батарею на остывание на пару часов
- Произвести замер плотности и при необходимости отрегулировать его снова
При повторной коррекции количество заменяемого электролита следует уменьшить.
Как приготовить самостоятельно
Перед тем, как самостоятельно заменить электролит для аккумулятора, необходимо принять соответствующие меры безопасности и приготовить предметы индивидуальной защиты:

- Перчатки
- Фартук
- Защитные очки
- Раствор соды на случай попадания средства на кожу или предметы одежды
- Уксус или лимонную кислоту – для нейтрализации щелочи
Проводить действия следует в хорошо проветриваемом помещении с температурой воздуха не выше +25 C°. Следует заранее знать, какой объем готового электролита потребуется для заполнения батарей. В среднем, в современных АКБ количество раствора составляет от 2,6 до 3,7 литра. Поэтому стоит сразу ориентироваться на максимальное количество. За основу можно взять 4 литра конечного раствора.
Для приготовления электролита необходимо заранее приготовить следующие предметы:
- Посуду достаточной емкости, изготовленную из материала, устойчивого к воздействию кислоты и щелочи
- Небольшую палочку для перемешивания электролита
- Инструменты для проведения замеров плотности, температуры и уровня раствора
- Для кислотного электролита – серную жидкость, для щелочного – щелочь в твердом или жидком виде, литий или силикагель
Важно! Все используемые материалы должны быть химически нейтральными для исключения возникновения ненужных реакций при их соприкосновении. В качестве емкости вполне подойдут обычные стеклянные банки.
Процесс приготовления щелочного электролита
Ингредиенты для приготовления данного состава могут быть как в жидком виде, так и в твердом. Если с первым все понятно, то перед тем как залить, щелочной электролит из твердого вещества потребуется развести в дистиллированной воде.
Требуемая плотность указывается на сайте производителя аккумулятора, также информацию можно найти в прилагаемой инструкции по эксплуатации. Твердый электролит берется пропорционально нужному количеству окончательного жидкого раствора и составляет:
- 1/5 – для получения раствора плотностью 1,17-1,19 г/м³
- 1/3 – для раствора плотностью 1,19-1,21 г/м³
- 1/2 — для раствора плотностью 1,25-1,27 г/м³
Процесс приготовления состоит из следующих шагов:
- Налить в посуду дистиллированную воду
- Добавить нужное количество щелочи
- Перемешать раствор
- Плотно закрыть крышкой
- Настаивать в течение 6 часов
После того, как процесс настаивания будет завершен, необходимо слить светлый раствор. Если часть состава выпадает в осадок, нужно его регулярно перемешивать. При заливке нужно следить, чтобы он остался на дне, не попав в аккумулятор, в противном случае это грозит выходом АКБ из строя.
Приготовление раствора для свинцовых аккумуляторов
Перед тем, как разбавить кислотный электролит, необходимо определить нужные пропорции. Они зависят от климатических условий, в которых планируется эксплуатация устройства.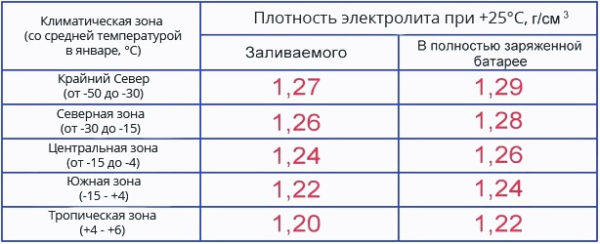
Для получения электролита плотностью 1,28 г/м³, что приемлемо для средних климатических условий, потребуется в один литр дистиллированной воды влить 0,36 л серной кислоты. Для жарких регионов количество серной кислоты уменьшается до 0,33 л на то же количество воды.
Как разводить аккумуляторную кислоту:
- Налить в подготовленную емкость дистиллированную воду
- Аккуратно тонкой струйкой влить в нее кислоту
- Измерить плотность полученного раствора
- Оставить раствор настаиваться на 12 часов
Важно! Нельзя вливать воду в кислоту! Правильно — вливать кислоту в воду. Не следует торопиться, вливая кислоту, давайте возможность ей постепенно раствориться в воде.
Инструкция по замене
Замена электролита производится в следующих случаях:
- Электролит в банках изменил цвет, стал мутным. Причиной тому может быть использование не дистиллированной воды для добавки, а обычно. Она может содержать примеси, вступающие в химическую реакцию с электролитом и образовывая твердые соединения, выпадающие в осадок
- После зарядки аккумулятора невозможно добиться нужной плотности
- Электролит вытек по неосторожности
- Новый аккумулятор быстро разряжается. Причиной тому может быть замерзание раствора

Замена электролита, независимо от того, является он щелочным или кислотным, производится в несколько шагов:
- Демонтаж аккумулятора из транспортного средства
- Очистка АКБ от загрязнений
- Выкачивание имеющейся жидкости с помощью груши или шприца
- Промывка банок дистиллированной водой
- Заливка электролита с помощью груши или аналогичных приспособлений
Уровень заливки определяется метками внутри банок. Если они отсутствуют, нужно руководствоваться правилом – электролит должен быть на уровне выше пластин на 5-7 миллиметров. При этом от его уровня до крышек банок должно оставаться не менее двух сантиметров.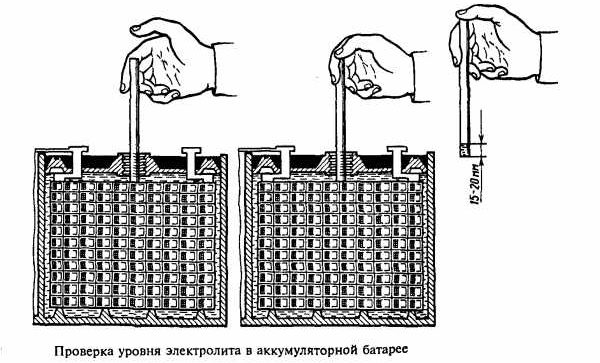
Очень важно при сливе электролита не наклонять его в сторону и тем более не переворачивать. На дне сосудов могут оказаться твердые частицы, которые застрянут в пластинах, полностью выведя их из строя. Допускается легкое покачивание воды из стороны в сторону при промывании, такие же действия можно производить после заливки электролита в аккумулятор.
После этого АКБ устанавливается на зарядку, после чего следует проверить получившуюся плотность. Замеры должны производиться не арене, чем через пару часов после снятия устройства с зарядки, так как существует риск получить завышенные показания. Если плотность недостаточно высокая или, напротив, имеет излишние значения, ее следует отрегулировать добавлением кислоты, щелочи или дистиллированной воды.
Полезное видео
Видео инструкция о замене электролита
Заключение
Независимо от типа электролита, используемого в эксплуатируемой АКБ, можно самостоятельно произвести его полную замену, проверку плотности и других показателей. Однако стоит помнить о технике безопасности, так как электролит – опасный химический состав, способный значительно повредить кожные покровы и глаза.
ЭЛЕКТРОЛИТ — это… Что такое ЭЛЕКТРОЛИТ?
электролит — электролит … Орфографический словарь-справочник
ЭЛЕКТРОЛИТ — (греч.). Жидкое тело, разлагаемое при помощи электрического (гальванического) тока. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. ЭЛЕКТРОЛИТ Жидкость, подверженная разложению посредством гальванического тока.… … Словарь иностранных слов русского языка
электролит — а, м. électrolyte m. < électro + гр. lytos разлагаемый. спец. Химическое вещество (в расплаве или растворе), способное разлагаться на составные части при прохождении через него электрического тока. Электролит аккумулятора. БАС 1. Швыряло… … Исторический словарь галлицизмов русского языка
электролит — Раствор, в котором при прохождении через него электрического тока происходит разложение вещества, которое приводит к появлению электрического тока. Электролит является основой аккумуляторов и батарей. [Гипертекстовый энциклопедический словарь по… … Справочник технического переводчика
ЭЛЕКТРОЛИТ — ЭЛЕКТРОЛИТ, электролита, муж. (от слова электрический и греч. lytos растворенный) (физ.). Раствор какого нибудь вещества, способного разлагаться на составные части при электролизе. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
электролит — сущ., кол во синонимов: 1 • католит (1) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
Электролит — Электролитами называют вещества, растворы и сплавыкоторых с другими веществами электролитически проводят гальваническийток. Признаком электролитической проводимости в отличие от металлическойдолжно считать возможность наблюдать химическое… … Энциклопедия Брокгауза и Ефрона
электролит — – вещество, водный раствор или расплав которого проводит электрический ток. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
ЭЛЕКТРОЛИТ — вещество, водный раствор или расплав которого проводит электрический ток (см.), образующимися в результате электролитической (см.). Этим Э., называемые также (см.) второго рода, отличаются от металлов (проводников первого рода), в которых перенос … Большая политехническая энциклопедия
Электролит — Электролит вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы, однако само вещество электрический ток не проводит. Примерами электролитов могут служить растворы кислот, солей и оснований.… … Википедия
Электролит — это… Что такое Электролит?
Электролитами называют вещества, растворы и сплавы которых с другими веществами электролитически проводят гальванический ток. Признаком электролитической проводимости в отличие от металлической должно считать возможность наблюдать химическое разложение данного вещества при более или менее продолжительном прохождении тока. В химически чистом состоянии Э. обыкновенно обладают ничтожно малой электропроводностью. Термин Э. введен в науку Фарадеем. К. Э. до самого последнего времени относили типичные соли, кислоты и щелочи, а также воду. Исследования неводных растворов, а также исследования при очень высоких температурах значительно расширили эту область. И. А. Каблуков, Кади, Карара, П. И. Вальден и др. показали, что не только водные и спиртовые растворы заметно проводят ток, но также растворы в целом ряде других веществ, как, например, в жидком аммиаке, жидком сернистом ангидриде и т. п. Найдено также, что многие вещества и смеси их превосходные изоляторы при обыкновенной температуре, как, например, безводные окислы металлов (окись кальция, магния и др.), при повышении температуры становятся электролитическими проводниками. Известная лампа накаливания Нернста, принцип которой был открыт гениальным Яблочковым, представляет превосходную иллюстрацию этих фактов. Смесь окислов — «тельце для накаливания» в лампе Нернста, не проводящая при обыкновенной темпер., при 700° делается превосходным и притом сохраняющим твердое состояние электролитическим проводником. Можно предположить, что большинство сложных веществ, изучаемых в неорганической химии, при соответствующих растворителях или при достаточно высокой температуре могут приобрести свойства Э., за исключением, конечно, металлов и их сплавов и тех сложных веществ, для которых будет доказана металлическая проводимость. В настоящий момент указания на металлическую проводимость расплавленного йодистого серебра и др. нужно считать еще недостаточно обоснованными. Иное должно сказать о большинстве веществ, содержащих углерод, т. е. изучаемых в органической химии. Вряд ли найдутся растворители, которые сделают углеводороды или их смеси (парафин, керосин, бензин и др.) проводниками тока. Однако и в органической химии мы имеем постепенный переход от типичных Э. к типичным неэлектролитам: начиная с органических кислот к фенолам, содержащим в своем составе нитрогруппу, к фенолам, не содержащим такой группы, к спиртам, водные растворы которых принадлежат к изоляторам при небольших электровозбудительных силах и, наконец, к углеводородам — типичным изоляторам. Для многих органических, а также отчасти и некоторых неорганических соединений, трудно ожидать, чтобы повышение температуры сделало их Э., так как эти вещества раньше разлагаются от действия теплоты.
В таком неопределенном состоянии находился вопрос о том, что такое Э., до тех пор, пока не привлечена для решения его теория электролитической диссоциации (см. соответствующую статью). Относительным числом электролитически диссоциированных молекул к не распавшимся молекулам и определяется, имеем ли мы дело с типичным Э. или с типичным неэлектролитом, или с каким-либо переходным случаем. Если число этих ионов настолько мало, что ни состав их, ни относительное число не поддается никаким измерительным методам, тогда перед нами случай типичного неэлекролита. Переходные случаи — это случаи, лежащие на границе наших измерительных методов, как чисто физических, так и применяемых при химическом анализе.
Интересный вопрос возник в самое последнее время: может ли быть простое тело Э.? П. И. Вальден нашел, что растворы брома в жидком сернистом ангидриде, растворы йода в эфире и треххлористом мышьяке заметно проводят ток. Должно ли признать, что молекула йода J2 распадается на ионы электроположительный катион J. и J’ — электроотрицательный анион. Однако, уже П. И. Вальден указывает на малую вероятность такого явления и предполагает, что бром и йод дают с растворителем определенные химические соединения, которые уже, в свою очередь, распадаются на ионы.
В заключение должно упомянуть об определении Э., данном маститым Гитторфом пятьдесят лет тому назад: «Э. — это соли». Этим определением Гитторф частью предвосхитил современную теорию электролитической диссоциации, указав на то, что типичное свойство солей, которое мы теперь определяем как способность к электролитической диссоциации, должно быть признаком всякого Э. (см. Электролитическая диссоциация).
Вл. Кистяковский.
Электролиты — это… Что такое Электролиты?
Электроли́т — химический термин, обозначающий вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы. Примерами электролитов могут служить кислоты, соли и основания. Электролиты — проводники второго рода, вещества, которые в растворе (или расплаве) состоят полностью или частично из ионов и обладающие вследствие этого ионной проводимостью.
Степень диссоциации
В растворах некоторых электролитов диссоциирует лишь часть молекул. Для количественной характеристики электролитической диссоциации было введено понятие степени диссоциации[1].
Классификация
Исходя из степени диссоциации все электролиты делятся на две группы
- Сильные электролиты — электролиты, степень диссоциации которых в растворах равна единице (то есть диссоциируют полностью) и не зависит от концентрации раствора. Сюда относятся подавляющее большинство солей, щелочей, а также некоторые кислоты.
- Слабые электролиты — степень диссоциации меньше единицы (то есть диссоциируют не полностью) и уменьшается с ростом концентрации. К ним относят воду, ряд кислот, основания p-, d-, и f-элементов.
Между этими двумя группами четкой границы нет, одно и то же вещество может в одном растворителе проявлять свойства сильного электролита, а в другом — слабого.
Использование термина «Электролит»
В естественных науках
Термин электролит широко используется в биологии и медицине. Чаще всего подразумевают водный раствор, содержащий те или иные ионы (напр., «всасывание электролитов» в кишечнике).
Электролиты в технике
Слово электролит широко используется в науке и технике, в разных отраслях оно может иметь различающийся смысл.
Электролит в электрохимии
Многокомпонентный раствор для электроосаждения металлов, а также травления и др. (технический термин, например, электролит золочения).
Электролит аккумуляторный
Обиходное название раствора серной кислоты для свинцовых аккумуляторов
Электролитический конденсатор
относящийся к типу «Электролитический», в котором в качестве одной из обкладок используется электролит. Конденсаторы данного типа, в отличии от других типов, обладают несколькими отличительными особенностями
- при очень маленьких габаритных размерах обладают на несколько порядков большей ёмкостью
- при проектировании электрических схем и при монтаже электролитов необходимо соблюдать полярность подключения, в противном случае они обязательно взрываются (в худшем случае) или просто вздуваются и вытекают (в лучшем)[2]
- работают на существенно низких частотах, в пределах всего лишь нескольких десятков кГц, конденсаторы большинства других типов могут работать на частотах до десятков, сотен, тысяч мГц и выше.
Примечания
- ↑ Степень дисссоциации (α) — отношение числа молекул, диссоциировавших на ионы к общему числу молекул растворенного электролита.
- ↑ Исключением являются специальные неполярные электролитические конденсаторы, которые представляют из себя два электролитических конденсатора в одном корпусе, включённые последовательно и обязательно встречной друг другу полярностью (плюс к плюсу или минус к минусу)
См. также
Wikimedia Foundation. 2010.
ЭЛЕКТРОЛИТ — это… Что такое ЭЛЕКТРОЛИТ?
электролит — электролит … Орфографический словарь-справочник
электролит — а, м. électrolyte m. < électro + гр. lytos разлагаемый. спец. Химическое вещество (в расплаве или растворе), способное разлагаться на составные части при прохождении через него электрического тока. Электролит аккумулятора. БАС 1. Швыряло… … Исторический словарь галлицизмов русского языка
электролит — Раствор, в котором при прохождении через него электрического тока происходит разложение вещества, которое приводит к появлению электрического тока. Электролит является основой аккумуляторов и батарей. [Гипертекстовый энциклопедический словарь по… … Справочник технического переводчика
ЭЛЕКТРОЛИТ — ЭЛЕКТРОЛИТ, раствор или расплав солей, способный проводить электрический ток и используемый для ЭЛЕКТРОЛИЗА (в ходе которого он разлагается). Ток в электролитах проводится заряженными частицами ИОНАМИ, а не электронами. Например, в свинцово… … Научно-технический энциклопедический словарь
ЭЛЕКТРОЛИТ — ЭЛЕКТРОЛИТ, электролита, муж. (от слова электрический и греч. lytos растворенный) (физ.). Раствор какого нибудь вещества, способного разлагаться на составные части при электролизе. Толковый словарь Ушакова. Д.Н. Ушаков. 1935 1940 … Толковый словарь Ушакова
электролит — сущ., кол во синонимов: 1 • католит (1) Словарь синонимов ASIS. В.Н. Тришин. 2013 … Словарь синонимов
Электролит — Электролитами называют вещества, растворы и сплавыкоторых с другими веществами электролитически проводят гальваническийток. Признаком электролитической проводимости в отличие от металлическойдолжно считать возможность наблюдать химическое… … Энциклопедия Брокгауза и Ефрона
электролит — – вещество, водный раствор или расплав которого проводит электрический ток. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
ЭЛЕКТРОЛИТ — вещество, водный раствор или расплав которого проводит электрический ток (см.), образующимися в результате электролитической (см.). Этим Э., называемые также (см.) второго рода, отличаются от металлов (проводников первого рода), в которых перенос … Большая политехническая энциклопедия
Электролит — Электролит вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы, однако само вещество электрический ток не проводит. Примерами электролитов могут служить растворы кислот, солей и оснований.… … Википедия
Электролит (химия) — это… Что такое Электролит (химия)?
- Электролит (химия)
Электроли́т — химический термин, обозначающий вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы. Примерами электролитов могут служить кислоты, соли и основания. Электролиты — проводники второго рода, вещества, которые в растворе (или расплаве) состоят полностью или частично из ионов и обладающие вследствие этого ионной проводимостью.
Степень диссоциации
В растворах некоторых электролитов диссоциирует лишь часть молекул. Для количественной характеристики электролитической диссоциации было введено понятие степени диссоциации[1].
Классификация
Исходя из степени диссоциации все электролиты делятся на две группы
- Сильные электролиты — электролиты, степень диссоциации которых в растворах равна единице (то есть диссоциируют полностью) и не зависит от концентрации раствора. Сюда относятся подавляющее большинство солей, щелочей, а также некоторые кислоты.
- Слабые электролиты — степень диссоциации меньше единицы (то есть диссоциируют не полностью) и уменьшается с ростом концентрации. К ним относят воду, ряд кислот, основания p-, d-, и f-элементов.
Между этими двумя группами четкой границы нет, одно и то же вещество может в одном растворителе проявлять свойства сильного электролита, а в другом — слабого.
Использование термина «Электролит»
В естественных науках
Термин электролит широко используется в биологии и медицине. Чаще всего подразумевают водный раствор, содержащий те или иные ионы (напр., «всасывание электролитов» в кишечнике).
Электролиты в технике
Слово электролит широко используется в науке и технике, в разных отраслях оно может иметь различающийся смысл.
Электролит в электрохимии
Многокомпонентный раствор для электроосаждения металлов, а также травления и др. (технический термин, например, электролит золочения).
Электролит аккумуляторный
Обиходное название раствора серной кислоты для свинцовых аккумуляторов
Электролитический конденсатор
относящийся к типу «Электролитический», в котором в качестве одной из обкладок используется электролит. Конденсаторы данного типа, в отличии от других типов, обладают несколькими отличительными особенностями
- при очень маленьких габаритных размерах обладают на несколько порядков большей ёмкостью
- при проектировании электрических схем и при монтаже электролитов необходимо соблюдать полярность подключения, в противном случае они обязательно взрываются (в худшем случае) или просто вздуваются и вытекают (в лучшем)[2]
- работают на существенно низких частотах, в пределах всего лишь нескольких десятков кГц, конденсаторы большинства других типов могут работать на частотах до десятков, сотен, тысяч мГц и выше.
Примечания
- ↑ Степень дисссоциации (α) — отношение числа молекул, диссоциировавших на ионы к общему числу молекул растворенного электролита.
- ↑ Исключением являются специальные неполярные электролитические конденсаторы, которые представляют из себя два электролитических конденсатора в одном корпусе, включённые последовательно и обязательно встречной друг другу полярностью (плюс к плюсу или минус к минусу)
См. также
Wikimedia Foundation. 2010.
- Электролиния Экибастуз-Кокчетав
- Электролиты
Смотреть что такое «Электролит (химия)» в других словарях:
электролит — – вещество, водный раствор или расплав которого проводит электрический ток. Общая химия : учебник / А. В. Жолнин [1] … Химические термины
Электролит — Электролит вещество, расплав или раствор которого проводит электрический ток вследствие диссоциации на ионы, однако само вещество электрический ток не проводит. Примерами электролитов могут служить растворы кислот, солей и оснований.… … Википедия
Наводороживание ПТК при катодной поляризации (i=1500 А/м2, электролит: 250±5 г/л K2CO3 +35±3 г/л) — Толщина платинового покрытия, мкм Длительность катодной поляризации, ч Температура, °С Содержание h3, мл/100 г металла 2,7 45 … Химический справочник
Числа переноса катионов в водных растворах при 25 °С — Электролит Эквивалентная концентрация, моль/л 0 0,01 0,02 0,05 0,1 0,2 … Химический справочник
Электрофоретическое поведение ионов CrO42-, Cu(II), Al(III), Fe(III), Cr(III) в 0,5 М растворах сульфатов — Электролит Движение, мм CrO42 Cu(II) Al(III) Fe(III) Cr(III) Na2SO4 … Химический справочник
Электрохимия — Электрохимия раздел химической науки, в котором рассматриваются системы и межфазные границы при протекании через них электрического тока, исследуются процессы в проводниках, на электродах (из металлов или полупроводников, включая графит) и… … Википедия
КОЛЛОИДЫ — КОЛЛОИДЫ, КОЛЛОИДНАЯ ХИМИЯ. Коллоиды (от греч. ко 11а клей, желатина), название, данное Грэмом (Graham) группе веществ, типичными представителями которых являются желатина или гум ми арабик. Коллоидная химия является наиболее молодой хим.… … Большая медицинская энциклопедия
Тетрахлороаурат(III) водорода — Общие Т … Википедия
Цезий — 55 Ксенон ← Цезий → Барий … Википедия
Литий — Запрос «Lithium» перенаправляется сюда; см. также другие значения. Эта статья о химическом элементе. О применении в медицине см. Препараты лития. 3 Гелий ← Литий … Википедия
Книги
- Неорганическая химия. Часть I. Поверхностные явления на границе оксид/электролит в кислых средах, Горичев Игорь Георгиевич, Атанасян Т. К., Якушева Е. А.. В данном пособии детально рассматриваются особенности кинетики растворения оксидов кобальта в кислых средах, адсорбция оксидов кобальта, причины возникновения двойного электрического слоя на… Подробнее Купить за 483 грн (только Украина)
- Неорганическая химия. Часть I. Поверхностные явления на границе оксид/электролит в кислых средах, Горичев Игорь Георгиевич, Атанасян Т. К., Якушева Е. А.. В данном пособии детально рассматриваются особенности кинетики растворения оксидов кобальта в кислых средах, адсорбция оксидов кобальта, причины возникновения двойного электрического слоя на… Подробнее Купить за 377 руб
- Неорганическая химия Часть I Поверхностные явления на границе оксид электролит в кислых средах Учебное пособие, Атанасян Т., Гричев И., Якушева Е.. В данном пособии детально рассматриваются особенности кинетики растворения оксидов кобальта в кислых средах, адсорбция оксидов кобальта, причины возникновения двойного электрического слоя на… Подробнее Купить за 262 руб


